Graphite
Le graphite est un minéral qui est, avec le diamant, la lonsdaléite et la chaoite, l'un des allotropes naturels du carbone ; c'est un élément natif qui se trouve en particulier dans les sédiments de métamorphisme régional mais, selon les roches,...
Recherche sur Google Images :

Source image : directindustry.fr Cette image est un résultat de recherche de Google Image. Elle est peut-être réduite par rapport à l'originale et/ou protégée par des droits d'auteur. |
Page(s) en rapport avec ce sujet :
- Définitions de graphite, synonymes, antonymes, dérivés de graphite, ... comme électrode, par exemple en sidérurgie (acier électrique) ;; comme cathode, ... (source : dictionnaire.sensagent)
- Le graphite est un minéral qui est , avec le diamant, la lonsdaleite et la chaoite, ... par exemple en sidérurgie (acier électrique) ;; comme cathode, ... (source : benoitclement.unblog)
| Graphite | |
|---|---|
 |
|
| Graphite | |
| Général | |
| Synonymes | C. I. 77265 C. I. Pigment Black 10 Mine de plomb Plombagine |
| No CAS | |
| No EINECS | |
| Apparence | flocons noirs, blocs, poudre ou copeaux[1]. |
| Propriétés physiques | |
| T° fusion | Point de sublimation : 3 652 °C[1] |
| Solubilité | dans l'eau : insoluble[1] |
| Masse volumique | 2, 09–2, 23 g·cm-3[1] |
| Cristallographie | |
| Classe cristalline ou groupe d'espace | R3m [2] |
| Paramètres de maille | a = 2, 460 Å b = 2, 460 Å |
| Volume | 280, 38 Å3 [2] |
| Densité théorique | 1, 707 [2] |
| Précautions | |
|
|
|
 |
|
|
|
|
 |
||
| Cet article est lié aux composés du fer et du carbone |
||
| Phases | ||
| Acier | ||
|
|
||
| Autre produits ferreux | ||
Le graphite est un minéral qui est , avec le diamant, la lonsdaléite et la chaoite, l'un des allotropes naturels du carbone ; c'est un élément natif qui se trouve en particulier dans les sédiments de métamorphisme régional mais, selon les roches, il peut se former aussi à partir du charbon organique, du magma ou par réduction des carbonates.
Sa structure est constituée de feuillets hexagonaux non compacts, appelés graphènes, scindés d'environ 0, 336 nm le long de la direction de leur normale. Dans chaque feuillet, chaque atome de carbone est fortement lié par des liaisons covalentes de type sigma pour ses 3 électrons sp2, et des liaisons covalentes de type π pour son autre électron p, Ces liaisons π sont des liaisons conjuguées avec les trois atomes voisins, les électrons y sont particulièrement mobiles ce qui explique la grande conductivité électrique et thermique mais aussi la couleur noir du graphite. Entre les feuillets les liaisons sont faibles de type Liaison de van der Waals, ce qui explique le clivage et la faible dureté.
Origine du nom
Le chimiste suédois Carl Wilhelm Scheele a découvert uniquement à la fin du XVIIIe siècle que ce minerai ne contenait pas de plomb, mais était une forme cristalline spécifique du carbone ; on l'appelait à l'époque plombagine et on l'utilisait pour écrire.
C'est le géologue allemand Abraham Gottlieb Werner qui a découvert le terme «graphite», s'inspirant du grec γράφειν (graphein = écrire).
Propriétés physiques
Le graphite est la forme stable du carbone à température ainsi qu'à pression ordinaires.
L'apparence du graphite est celle d'un solide noir à l'éclat submétallique ; sa dureté est faible, entre 1 et 2 sur l'échelle de Mohs.
À cause de sa structure en feuillets, l'ensemble des propriétés physiques du graphite sont anisotropes. Surtout, la conductivité électrique est particulièrement différente dans le plan des feuillets et dans la direction perpendiculaire.
Polytypisme
Le graphite existe en deux polytypes :
- graphite-2H, système cristallin hexagonal, classe cristalline dihexagonale-bipyramidale, groupe d'espace P 63/mmc, empilement de type ABAB où le plan B est translaté de
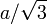 comparé au plan A. Quoique sa structure soit analogue à celle des métaux qui cristallisent avec empilement hexagonal compact, le graphite est un non-métal. Il possède une certaine conductivité électrique, sa résistivité électrique est de 50 µΩ. m, soit 2900 fois celle du cuivre.
comparé au plan A. Quoique sa structure soit analogue à celle des métaux qui cristallisent avec empilement hexagonal compact, le graphite est un non-métal. Il possède une certaine conductivité électrique, sa résistivité électrique est de 50 µΩ. m, soit 2900 fois celle du cuivre. - graphite-3R, trigonal à réseau rhomboédrique, empilement de type ABCABC. La structure rhomboédrique est instable : elle se produit par moulage et disparaît lors d'un recuit. On ne la trouve jamais comme forme pure, mais uniquement comme tendance à l'empilement ABC dans les cristaux hexagonaux primaires.
Le charbon existe dans l'ensemble des états intermédiaires entre charbon amorphe et graphite hexagonal. On parle de graphite «lubricostratique» (latin «lubrico» rendre glissant) lorsque les couches sont déplacées parallèlement au hasard, et de graphite «turbostratique» (latin «turbo» tourbillon) si elles sont aussi tournées au hasard.
Utilisations
Le graphite a de nombreuses applications industrielles, sous diverses formes naturelles ou synthétiques :
- construction mécanique : pièces de frottement, joints d'étanchéité, produits lubrifiants ;
- construction électrique : balais de moteurs ;
- comme réducteur, surtout en sidérurgie (coke des hauts-fourneaux) ;
- comme électrode, par exemple en sidérurgie (acier électrique) ;
- comme cathode, par exemple dans l'industrie d'électrolyse de l'aluminium ;
- comme modérateur dans des réacteurs nucléaires ;
- comme adsorbant, dans les filtres à «charbon actif».
- comme conducteur électrique (Pencil Mod)
Il est aussi utilisé en médecine comme absorbant en cas d'intoxication par voie orale.
Dans les arts plastiques, il est utilisé pour le dessin. Il sert surtout à fabriquer des crayons, fréquemment sous l'appellation incorrecte de «mine de plomb».
L'utilisation domestique la plus courante est le crayon à papier.
Aussi peut-il être utilisé comme composite d'alliage (Titane / Fibre de verre / Aluminium) dans la fabrication des cadres de raquettes de tennis.
Une forme pyrolytique du graphite est utilisée dans la fabrication de grilles pour les tétrodes de très grande puissance dans le domaine de la radiodiffusion. On peut citer par exemple la tétrode TH539 qui a été utilisée jusqu'en mars 2003 sur l'un des deux blocs émetteurs ondes longues d'Allouis de 1 000 kW.
Références
- GRAPHITE (NATUREL) , fiche de sécurité du Programme International sur la Sécurité des Substances Chimiques, consultée le 9 mai 2009
- Graphite sur www. reciprocalnet. org. Consulté le 12 décembre 2009
- «Graphite naturel» dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 09/12/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.


 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité