Platine
Le platine est un élément chimique, de symbole Pt et de numéro atomique 78.
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Informations générales | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Nom, Symbole, Numéro | Platine, Pt, 78 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Série chimique | métal de transition | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Groupe, Période, Bloc | 10, 6, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse volumique | 21, 45 g·cm-3 (20 °C) [1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dureté | 3, 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Couleur | blanc-gris | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N° CAS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N° EINECS | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés atomiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse atomique | 195, 084 ± 0, 009 u[1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon atomique (calc) | 135 pm (177 pm) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de covalence | 1, 36 ± 0, 05 Å [2] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Rayon de Van der Waals | 175 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Configuration électronique | [Xe]4f145d96s1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électrons par niveau d'énergie | 2, 8, 18, 32, 17, 1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État (s) d'oxydation | 2, 4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Oxyde | basique | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure cristalline | cubique face centrée | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| État ordinaire | solide | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point de fusion | 1 768, 2 °C [1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point d'ébullition | 3 825 °C [1] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de fusion | 19, 6 kJ·mol-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergie de vaporisation | 510 kJ·mol-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume molaire | 9, 09×10-6 m3·mol-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pression de vapeur | 31, 2 mPa | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | 2 680 m·s-1 à 20 °C | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Divers | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Électronégativité (Pauling) | 2, 28 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Chaleur massique | 130 J·kg-1·K-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité électrique | 9, 66×106 S·m-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Conductivité thermique | 71, 6 W·m-1·K-1 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilité | sol. dans eau régale[3] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Énergies d'ionisation[4] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1re : 8, 9588 eV | 2e : 18, 563 eV | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Isotopes les plus stables | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Produit non contrôlé | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI & CNTP, sauf indication contraire. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Le platine est un élément chimique, de symbole Pt et de numéro atomique 78.
C'est un métal de transition dur, malléable, ductile, rare et par conséquent précieux, de couleur gris-blanc. Le platine est un métal noble résistant à la corrosion, et on le trouve fréquemment associé certains minerais de cuivre ou de nickel, et plus rarement sous forme de dépôt natif (en Afrique du Sud en particulier).
Il est utilisé en bijouterie, dans les équipements de laboratoire, en médecine dentaire et pour la réalisation de fausses dents en alliage or-platine, pour certains contacts électriques et en particulier dans les pots catalytiques des véhicules.
Histoire
Présent dans la nature, le platine et ses alliages sont connus depuis longtemps.
Ce métal était utilisé par les Indiens précolombiens, et la première référence européenne apparut en 1557 dans les écrits de l'humaniste italien Julius Cæsar Scaligero (1484-1558) qui le décrivit comme un métal mystérieux venant de mines localisées entre Darién (Panama) et Mexico.
Les Espagnols nommèrent le métal platina (petit argent) lorsqu'il s le découvrirent en Colombie. Ils le considéraient alors comme une impureté de l'argent et ne le conservaient pas.
Le platine fut découvert par les astronomes Antonio de Ulloa et don Jorge Juan y Santacilia (1713-1773), qui tous deux avaient été appointés par le roi Philippe V d'Espagne pour rejoindre une expédition géographique au Pérou qui dura de 1735 à 1745. Parmi d'autres choses, Ulloa observa le platina del pinto, un métal inexploitable trouvé avec l'or de Nouvelle-Grenade (Colombie).
Des corsaires britanniques interceptèrent le navire d'Ulloa sur le chemin du retour. Quoiqu'il fût bien traité en Angleterre et admis comme membre de la Royal Society, on l'empêcha de publier une référence aux métaux inconnus avant 1748. Avant que cela ne puisse arriver, Charles Wood isola indépendamment l'élément en 1741.
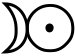
Le symbole alchimique du platine (ci-contre) a été créé par fusion des symboles de l'argent et de l'or.
Le platine est désormais reconnu comme un métal plus précieux que l'or, de telle sorte qu'une récompense de platine est meilleure qu'une récompense d'or. Le prix du platine fluctue selon sa disponibilité, mais normalement il coûte à peu près deux fois plus cher que l'or.
La définition standard d'un mètre fut longtemps basée sur la distance entre deux marques sur une barre de platine iridié conservée au Bureau international des poids et mesures à Sèvres en France. Actuellement un cylindre de platine iridié, aussi conservé au BIPM, sert de prototype au kilogramme.
Le platine est aussi utilisé dans la définition de l'électrode standard à hydrogène.
Propriétés
Ce métal a une couleur argent-blanc quand il est pur, il est malléable, ductile et particulièrement résistant à la corrosion.
Sa résistance à l'abrasion et au ternissement font qu'il est apprécié en bijouterie.
Le platine interagit avec de nombreuses molécules, ce qui en fait un catalyseur particulièrement recherché. À température ambiante, il résiste cependant à de nombreuses attaques chimiques : il ne s'oxyde pas à l'air libre, et n'est corrodé que par les cyanures, les halogènes, le soufre et les métaux alcalins caustiques. Sauf à l'état de micro- ou nanoparticules, il est insoluble dans l'acide chlorhydrique et dans l'acide nitrique, mais il se dissout dans l'eau régale (mélange de ces deux acides). À haute température (à partir de 600 °C), il réagit avec le dioxygène de l'air pour former un oxyde volatil (PtO2), oxyde lamellaire stable[6], qui a aussi un pouvoir catalytique (catalyseur d'Adams), et qui peut être réduit en platine colloïdal par le dihydrogène in situ.
Les caractéristiques catalytiques du platine, comme celles des six autres métaux du groupe du platine, sont exceptionnelles.
A titre d'exemple, un mélange de dihydrogène et de dioxygène explose en présence de platine : le platine catalyse la réaction qui est exothermique, l'élévation de température consécutive provoque alors un emballement de la réaction, d'où l'explosion. Sous certaines formes, le platine est un puissant toxique (il détruit l'ADN en empêchant la double hélice de se dérouler), ce pourquoi il est utilisé pour traiter certains cancers (chimiothérapie) en bloquant le processus de division rapide normal de certaines cellules (dont celles qui font pousser les cheveux, d'où une chute des cheveux lors de certaines chimiothérapies).
Isotopes
Le platine naturel est un mélange de cinq isotopes stables et d'un isotope radioactif, le 190Pt, de très longue période radioactive (650 milliards d'années). Il existe aussi de nombreux autres radioisotopes dont le plus stable est le 193Pt dont la période est de 50 ans.
Gisements et production
Le platine se trouve généralement à l'état natif et le minerai de sperrylite (arséniure de platine, PtAs2) est la source principale du métal. L'alliage platine/iridium naturel est le platiniridium et se trouve aussi dans le coopérite minéral (sulfure de platine, PtS).
Le platine, fréquemment accompagné de faibles quantités d'autres métaux de la famille du platine, peut être trouvé dans certaines alluvions ; en Afrique du Sud où il est aussi fortement concentré dans le complexe magmatique de Bushveld (environ 5 g/t), Colombie, en Ontario, dans l'Oural et dans certains états de l'ouest des États-Unis d'Amérique. En Europe, il est extrait dans le grand nord de la Russie, dans les gisements de cuivre et nickel de la presqu'île de Taïmyr, dans le complexe métallurgique et minier de Norilsk créé par la Russie soviétique en 1935 (en 1953, on y produisait déjà 35 % du nickel de l'Union Soviétique, 30 % du cobalt et 90 % des métaux du groupe du platine, ou «platinoïdes»). Cette activité est à l'origine de la ville de Norilsk (175 000 habitants) et d'une voie ferrée qui transporte le minerai vers le port de Dudunka sur l'Ienisseï puis vers l'usine Severonickel dans la presqu'île de Kola. 330 000 t de nickel ont été extraites du sol rien qu'en 2003 (c'est 23, 6 % de la production mondiale). C'est du même minerai qu'est tiré le platine, qui y est présent en faible quantité[7].
Le platine est le plus fréquemment produit commercialement comme sous-produit du traitement du minerai de nickel, qui en contient deux grammes par tonne.
| Pays | Tonnes | % du total |
|---|---|---|
| Afrique du Sud | 148, 3 | 75, 8 |
| Russie | 29, 6 | 15, 1 |
| Canada | 7, 4 | 3, 8 |
| Zimbabwe | 4, 4 | 2, 2 |
| États-Unis | 4, 1 | 2, 1 |
| Total 5 pays | 193, 8 | 99, 0 |
| Total monde | 195, 7 | 100, 0 |
Chiffres de 2003, métal contenu dans les minerais et concentrées, source : L'état du monde 2005
En 2008, l'offre mondiale était de 198 tonnes réparties comme suit[8] :
- 170 tonnes proviennent de l'extraction minière,
- 28 tonnes issues du recyclage des catalyseurs automobiles.
Utilisation
Le platine est particulièrement utilisé en bijouterie, dans les contacts électriques, dans les creusets et dans les fourneaux électriques à haute-température. Avec deux autres métaux du groupe du platine, il est fréquemment utilisé comme catalyseur chimique et surtout dans les pots catalytiques de moteurs à combustion interne des véhicules et dans différents procédés industriels, quoiqu'il tende à être remplacé par du palladium (aussi de plus en plus utilisé dans les catalyseurs diesel[8]). Voici d'autres utilisations :
- Il peut adsorber une grande quantité de dihydrogène, qu'il relâche quand il est chauffé. Son utilisation dans la conception d'un conteneur d'hydrogène associé à des piles à combustible est à l'étude.
- L'industrie chimique utilise une quantité significative de platine ou d'alliage platine-rhodium sous forme de gaze (filet fin) pour catalyser l'oxydation partielle de l'ammoniac pour produire de l'oxyde nitrique, qui entre dans la composition d'engrais, d'explosifs et de l'acide nitrique.
- Des catalyseurs au platine sont utilisés dans le raffinage et la transformation du pétrole, mais aussi dans d'autres processus de la production d'essence et de composés aromatiques dans l'industrie pétrochimique.
- Ce métal a un cœfficient de dilatation presque égal à celui du verre de silicate sodocalcique et est par conséquent utilisé pour sceller des électrodes dans du verre.
- Les alliages de platine et cobalt ont d'excellentes propriétés magnétiques. Un alliage de 76, 7 % de platine et 23, 3 % de cobalt, en masse, forme un aimant extrêmement puissant.
- L'alliage platine/osmium 90/10 est utilisé pour réaliser des stimulateurs cardiaques, des valvules cardiaques artificielles ou d'autres implants.
- Utilisé pour recouvrir le nez des missiles, les injecteurs des moteurs à réaction et des systèmes qui doivent pouvoir fonctionner durablement à haute température.
- Un fil de platine fin porté à incandescence est un catalyseur de la réaction de transformation du méthanol (vapeur) en formaldéhyde. Ce phénomène a eu une application commerciale dans la fabrication de briquets ou de chaufferettes à alcool.
- Le cisplatine [PtCl2 (NH3) 2] et le carboplatine sont certaines des substances les plus efficaces dans le traitement de certains types de cancer dont la leucémie, le cancer du testicule ou le cancer de la vessie.
- Sa résistivité variant selon la température, il est utilisé pour les thermomètres à résistance de platine et pour produire des thermocouples, sous la forme d'une soudure entre du platine pur et du platine rhodié.
- Il est utilisé sous forme de pots, creusets et coupelles dans les laboratoires pharmaceutiques et de chimie industrielle.
- Le platine est utilisé dans la photographie : la platinotypie est un processus de tirage photographique breveté par William Willis en 1873.
Les qualités du platine en font l'une des huit matières premières stratégiques reconnues comme indispensables en temps de guerre comme en temps de paix[9].
Économie
Production
Les principaux producteurs mondiaux de platine sont[10] :
- Anglo American : près de 70 tonnes produites en 2007,
- Impala Platinum (Afrique du Sud) : près de 55 tonnes,
- Lonmin (ex-Lonrho) : à peu près 22 tonnes,
- Norilsk Nickel : à peu près 20 tonnes.
Impacts écologiques et toxicologiques
Lorsqu'il est pur et massif, le platine ne pose a priori aucun problème de santé environnementale.
Mais depuis qu'il est abondamment utilisé comme catalyseur, on commence à le trouver dans l'ensemble des compartiments de l'environnement et surtout dans l'air urbain[11]. La pluie lessive l'air, et les eaux de ruissellement l'apportent aux stations d'épuration urbaine, où il s'ajoute à celui qui provient des urines (dont celles de patients traités contre le cancer), des excréments et de certains rejets industriels. Dès le milieu des années 1990, on le retrouvait dans des boues d'épuration, avec des variations importantes liées à la météo (il y en a moins lorsque le temps est sec, et plus lorsqu'il est pluvieux[12]). Localement, l'industrie est une source qui, pour ce qui concerne la contamination des eaux usées, dépasse les apports automobiles (ça a été vérifié dans une grande zone industrielle de Munich[12]). Comparées à ceux des analyse de boues d'épuration de 15 stations d'épuration de petites villes rurales allemandes, les taux de platine des boues d'épuration munichoises étaient nettement plus élevés[12].
Le taux de platine augmente jusque dans l'urine humaine et tous ses composés sont hautement toxiques.
Sous leurs formes biodisponibles, les platinoïdes se sont montrés bio-assimilables chez les plantes et animaux expérimentalement exposés. Ceci a été démontré chez diverses plantes terrestres ou aquatiques, pour des composés solubles et pour des particules liées au platine, au palladium et au rhodium[13].
Le platine des pots catalytiques, rare et coûteux tend à être remplacé par le palladium (ou associé à ce dernier). Dans les mêmes conditions, le palladium semble aussi bio-assimilable que le platine, ou alors plus que ce dernier.
- Le palladium et le platine ont été dosés chez 22 espèces d'algues du littoral californien, avec une technique analytique nouvelle, particulièrement sensible[14] ; les teneurs dans ces algues variaient de 0, 09 à 0, 61 ng/g pour le palladium et 0, 25 à 1, 75 ng/g pour le platine (en matière sèche) [14].
- Le ratio moyen de Pt/Pd trouvé dans ces algues était de 3, 5 tandis qu'il était de 4, 5 dans la mer. On suppose par conséquent que ces algues accumulent le palladium et le platine de l'eau de mer, sans discrimination, à cause de la similitude chimique de ces métaux[14].
Chez les animaux (espèces aquatiques essentiellement) expérimentalement exposés à des sels solubles ou à des substances catalytiques, la bioconcentration est aussi démontrée[13].
- A titre d'exemple, le platine sous forme de H2PtCl6 provoque chez le poisson Danio rerio une lyse et nécrose des cellules de la muqueuse intestinale, des changements dans la sous-muqueuse, et la fusion des villosités entre elles[15]. Cet effet était d'autant plus marqué que la concentration ou le temps d'exposition était élevé. Lors d'une exposition de 15 jours à une concentration sublétale de 16 µg/L, suivie d'un période de non-exposition de 64 jours, ces lésions étaient cependant réversibles.
- Les animaux filtreurs y sont surtout vulnérables : à titre d'exemple et de comparaison avec d'autres "métaux lourds", pour la moule zébrée (Dreissena polymorpha) vivant en eau douce, la biodisponibilité des platinoïdes issus de poussières routières se situe entre celle du cadmium et du plomb[13], avec, on peut on supposer, des effets synergiques.
Des vers parasites des poissons ont aussi montré une capacité à bioaccumuler les platinoïdes (ils pourraient par conséquent être utile à la biosurveillance fine de milieux aquatiques[13].
La bioassimilabilité et bioconcentration sont aussi observées lorsque ce sont des sédiments de rivières urbaines, de la poussière routière ou de tunnel qui sont utilisés comme sources de platinoïdes pour l'expérience[13].
Parmi les platinoïdes, le platine semble moins bio-assimilable que le palladium, pour la faune comme pour la flore[13]. Cependant, sous forme de micro ou nanoparticules, le platine devient particulièrement actif, même à particulièrement faible dose.
Les composés du platine biodisponibles étaient particulièrement rares dans la nature. Mais ils sont désormais produits en grandes quantités par l'industrie et beaucoup répandus dans l'environnement, surtout via l'incinération, l'épandage de boues d'épuration[12] et lors du vieillissement des pots catalytiques.
- A titre d'exemple, des analyses de 166 échantillons d'air et des urines de 178 personnes (non exposées par leur profession) ont été faites à Munich de 1993 à 1996. Elles ont montré une très forte augmentation (triplement) des teneurs de l'air en 3 ans (passant de 7, 3 ± 6, 5 pg/m3 en 1993-1994 à 21, 5 ± 13, 8 pg/m3 pour 1995-1996), avec jusqu'à 62 pg/m3. Le taux moyen de platine urinaire pour les 178 personnes était de 6, 5 ng/g de créatinine. La distribution anormale de ce platine dans la population (96% des personnes testés avaient moins de 20 ng/g de créatinine (SD = 6, 4; MEDIAN 4, 3 =; MAX = 45 ng/g de créatinine) tandis que quelques personnes en présentaient 3 à 4 fois plus. L'étude a montré que ces derniers étaient en fait contaminés par des alliages dentaires or-platine qu'ils portaient[16].
- On en trouve une quantité croissante dans les poussières des zones où la circulation automobile est importante. Par exemple à Mexico où les véhicules n'ont commencé à être équipés de pots catalytiques qu'en 1991[17].
- Il en allait de même à Boston aux USA, les taux de platinoïdes sont en forte augmentation parmi les particules PM10 inhalées par la population[18].
- En Italie[19], dans le sol de Naples et d'une zone périphérique de 120 km2, les taux de platine et de palladium (dosés dans 195 échantillons) variaient de moins de 2 μg/kg à 52 μg/kg pour le platine et de moins de 10 μg/kg à 110 μg/kg pour le palladium. Or, les teneurs sont reconnues comme anormales au dessus de 6, 2 μg/kg de platine et de 17, 2 μg/kg de palladium.
Plus la circulation était intense, plus le taux de ces métalloïdes était élevé.
La cartographie de la pollution était fortement corrélée à celle du réseau routier et de la densité de circulation[19].
Bien qu'ils ne soient obligatoires en Europe que depuis 1993 l'identité et les proportions respectives de platinoïdes (Pt / Pd / Rh) correspondent à celles des pots d'échappement catalytiques, ce qui laisse supposer qu'ils sont bien à l'origine des valeurs de plus en plus élevées (même en Italie où l'État a autorisé les pots non-catalytiques jusqu'en janvier 2002[19]. ). - Les tunnels sont des zones où l'air est - plus qu'ailleurs- «enrichi» en particules de platinoïdes de petite et particulièrement petite taille (PM10 and PM2.5) [20], ce qui laisse penser qu'elles peuvent pour partie passer dans le sang via les poumons. Dans un tunnel étudié en Autriche, les taux variaient selon le point de prélèvement (distance comparé à l'entrée), le taux de renouvellement de l'air par la ventilation, et le nombre de véhicules empruntant le tunnel. Les taux variaient de 38 ± 5, 9 à 146 ± 13 ng émis en moyenne par véhicule et kilomètre, tandis que les facteurs d'émission de palladium variaient de 13 ± 2, 1 à 42 ± 4, 1 ng. veh-1. km-1. La plus grande partie du Pt et Pd étaient présent forme d'aérosol dont la taille particulaire dépassait le PM10, mais 12% et 22% respectivement de ces platinoïdes était émis sous forme de particules assez fines (PM2) [20] pour être inhalées et passer dans le dispositif sanguin et d'autres organes.
- Les platinoïdes ont aussi augmenté dans les sédiments de rivières ou de lacs. A titre d'exemple, dans un lac proche de Boston[21].
- L'analyse de 3 platinoïdes (Pt, Pd, Rh) dans les couches de sédiment montre une nette augmentation depuis la naissance des pots catalytiques (teneurs 6 à 16 fois plus importantes en 1992-2002 qu'avant l'introduction des catalyseurs) [21]. Les rapports de proportion entre ces éléments signent leur origine automobile (c'est la même que celle de ces produits dans les pots catalytique des à peu près 500 million de véhicules équipés de pots catalytiques circulant dans le monde vers 2004. Les teneurs en iridium et le ruthénium (Ru) ont aussi augmenté après l'introduction des catalyseurs[21].
- Le platine, le palladium et le rhodium ont été dosés dans des échantillons de neige fraîche prélevés à 14 lieux de la vallée d'Aspe (Pyrénées, France) durant deux hivers, (février 2003 et mars 2004) [22]. Les limites de détection étaient de 0, 05, 0, 45, et 0, 075 pg/g respectivement pour le Pt, Pd et Rh[22].
La neige fraîche contenait de 0, 20 à 2, 51 pg/g pour le Pt, de 1, 45 à 14, 04 pg/g pour le palladium et de 0, 24 à 0, 66 pg/g pour Rh. les teneurs les plus élevées étaient dans la majorité des cas trouvées près des axes routiers, sans lien direct ou évident avec le trafic routier. Durant l'étude la direction et l'origine des masses d'air atteignant la vallée ont été enregistrées, de façon à apporter des indices sur l'origine de ces platinoïdes[22].
Les teneurs étaient plus élevées en 2004 qu'en 2003. Les auteurs estiment que les platinoïdes trouvés dans la neige des pyrénées en 2004 provenait du parc des véhicules européens, et de certaines activités minières russes[22]. - Le taux de platine et platinoïdes catalytiques mesuré dans les neiges et glaces du pôle Nord a fortement augmenté entre 1990 et 2000 ; et les taux mesurés dans les couches de neige constituées au milieu des années 1990 sont 40 à 120 fois plus élevés que ceux mesurés dans la glace datant de 7000 ans, ce qui indique une contamination à large échelle de toute la troposphère de l'hémisphère Nord par les platinoïdes. Ici aussi, le rapport massique Pt/Rh des échantillons de neige la plus récente est proche du rapport moyen de ces catalyseurs dans les pots catalytiques, ce qui suggère aux auteurs de cette étude «qu'une grande partie de l'augmentation récente du Pt et Rh pourrait provenir de convertisseurs catalytiques d'automobiles»[23].
- Tandis que la contamination par l'osmium (Os) était jadis associée aux tanneries, les changements récents de composition isotopique de l'osmium (aussi présent dans les pots catalytiques neufs, comme impureté) montrent une autre source anthropique pour cet élément. L'hypothèse que les catalyseurs automobiles sont une source d'iridium et d'osmium est toujours renforcée par le fait que ces éléments sont les plus concentrés dans la poussière de tunnels routiers[21].
Bien que leur potentiel toxicologique et écotoxicologique soit toujours mal connu, et qu'on n'ait pas encore détecté d'effets écologiques majeurs ou aigus attribuables avec certitude à ces platinoïdes anthropiques[13], des effets chroniques sur la biosphère sont suspectés, surtout car[13] :
- sous forme de très petites particules, ce sont de puissants catalyseurs ;
- leur augmentation est rapide et cumulative (effets synergiques potentiels) ;
- leur augmentation semble déjà concerner l'ensemble des compartiments de l'environnement, et au moins tout l'hémisphère-nord[24] ;
- leur disponibilité biologique est énormément plus importante qu'on ne le pensait il y a quelques décennies ;
- leur bioaccumulation est avérée pour de nombreuses espèces et plausible pour les autres.
La question d'éventuels effets sanitaires - via l'alimentation ou via l'inhalation de particules - se pose par conséquent.
Dans l'ensemble des cas, les études sont compliquées par les difficultés techniques d'analyse des traces de Pt, Pd et Rh (bien que des techniques récentes permettent des mesures particulièrement précises en Pg/g d'échantillon) et en particulier par d'importantes lacunes en matière de connaissance de leurs impacts environnementaux[13], [25].
De plus, les émissions (industrielles ou des pots catalytiques) changent dans leur composition. A titre d'exemple, à Mexico, on a noté un pic en 1993, puis une moindre augmentation des taux de Pt-Pd-Rh[17], ce qui suggère que les premiers pots catalytiques perdaient plus rapidement qu'aujourd'hui une partie de leurs catalyseurs, soit parce que la technologie ne permettait pas une bonne adhésion des catalyseurs à la matrice du pot, soit parce que les conducteurs utilisaient des carburants inappropriés, ou pour ces deux raisons à la fois.
Symbolique
- Les noces de platine symbolisent les 70 ans de mariage dans la tradition française (symbole de stabilité).
- Le platine est le 12e niveau dans la progression de la sarbacane sportive.
- Le disque de platine est une récompense honorifique remise aux artistes ayant atteint le million d'albums vendus.
- Sur les jeux PlayStation 3, un trophée (virtuel) de platine est obtenu après qu'un joueur a obtenu l'ensemble des trophées de bronze, d'argent et d'or du jeu.
Autres significations
Dans le monde financier, le terme platine fait référence au téléphone utilisé dans une salle de trading ou d'arbitrage par les opérateurs de marchés financiers (traders). Il sert à communiquer avec la plupart de contre-parties (60) sur des dispositifs combinant haut-parleurs et micros mais aussi sur 2 à 6 combinés. Cette industrie traverse une révolution technologique passant de dispositifs digitaux à des dispositifs de type IP (Internet Protocol). De nouveaux leaders émergent, tels IP Trade, qui font concurrence aux acteurs en place : Etrali, IPC et BT.
Voir aussi
Références
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, 2009, 90e éd. , Relié, 2804 p. (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, «Covalent radii revisited», dans Dalton Transactions, 2008, p. 2832 - 2838 [ lien DOI ]
- (en) Metals handbook, vol. 10 : Materials characterization, ASM International, 1986, 1310 p. (ISBN 0-87170-007-7) , p. 344
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, 2009, 89e éd. , p. 10-203
- «Platine» dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Extrait de la thèse Équilibres oxydo-réducteurs dans les dichalcogénures de platine et de palladium. Influence de la pression sur la redistribution du nuage électronique de Céline Sortais-Soulard
- Note du BRGM pour le ministère de l'Industrie français
- Li, Ni, Pt, Pd : des métaux "critiques" ? ; notes de synthèse, rédigées par des experts d'IFP Energies nouvelles (PDF - 700 Ko)
- Avec le germanium (électronique avancée) ; le titane (sous-marins de chasse, alliage extrêmement résistant ; le magnésium (explosifs) ; le mercure (chimie nucléaire, instruments de mesure) ; le molybdène (acier) ; le cobalt (chimie nucléaire) ; le colombium (alliages spéciaux extrêmement rares). (Christine Ockrent, comte de Marenches, Dans le secret des princes, éd. Stock, 1986, p; 193. )
- Financial Times, 7 août 2008, page 14
- F. Alt, A. Bambauer, K. Hoppstock, B. Mergler and G. Tölg ; Platinum traces in airlimite particulate matter. Determination of whole content, particle size distribution and soluble platinum ; Fresenius'Journal of Analytical Chemistry ; Volume 346, Numbers 6-9, 693-696, DOI :10.1007/BF00321274 ; (Springerlink)
- Dagmar Laschka, Markus Nachtwey ; Platinum in municipal sewage treatment plants ; Chemosphere, Volume 34, Issue 8, April 1997, Pages 1803-1812
- Sonja Zimmermann & Bernd Sures ; 2004 ; Significance of platinum group metals emitted from automobile exhaust gas converters for the biosphere Sonja Zimmermann and Bernd Sures ; Environmental Science and Pollution Research Volume 11, Number 3, 194-199, DOI : 10.1007/BF02979675
- Jæ Sam Yang, Determination of palladium and platinum in seaweed ; Journal of Oceanography ; Volume 45, Number 6, Journal of Oceanography, 1989, Volume 45, Number 6, Pages 369-374 ; DOI : 10.1007/BF02125141
- R. Jouhaud, S. Biagianti-Risbourg, F. Arsac et G. Vernet ; Journal of Applied Ichthyology ; Volume 15, Issue 1, pages 41–48, Mars 1999; online : 2002/04/05 ; Résumé DOI : 10.1046/j. 1439-0426.1999.00114. x
- Rudi Schierl ;Environmental monitoring of platinum in air and urine ; Microchemical Journal, Volume 67, Issues 1-3, December 2000, Pages 245-248, doi :10.1016/S0026-265X (00) 00068-0 (Résumé)
- Sebastien Rauch, Bernhard Peucker-Ehrenbrink, Luisa T. Molina, Mario J. Molina, Rafæl Ramos, and Harold F ; Platinum Group Elements in Airlimite Particles in Mexico City. Hemond Environmental Science & Technology ; 2006 40 (24), 7554-7560
- Sebastien Rauch, Harold F. Hemond, Bernhard Peucker-Ehrenbrink, Kristine H. Ek, and Gregory M. Morrison ; Platinum Group Element Concentrations and Osmium Isotopic Composition in Urban Airlimite Particles from Boston, Massachusetts, Environmental Science & Technology ; 2005 39 (24), 9464-9470
- Cicchella D., De Vivo B. and Lima A ; [Palladium and platinum concentration in soils from the Napoli metropolitan area], Italy : envisageable effects of catalytic exhausts, The Science of the Total Environment, 308 : 121-131, online 21 February 2003.
- Andreas Limbeck, Christoph Puls, and Markus Handler ; [Platinum and Palladium Emissions from On-Road Vehicles in the Kaisermühlen Tunnel (Vienna, Austria) ] ; Environmental Science & Technology ; 2007 41 (14), 4938-4945
- Sebastien Rauch, Harold F. Hemond, & Bernhard Peucker-Ehrenbrink ; Recent Changes in Platinum Group Element Concentrations and Osmium Isotopic Composition in Sediments from an Urban Lake ; Environ. Sci. Technol., 2004, 38 (2), pp 396–402 ; DOI : 10.1021/es0347686
- Mariella Moldovan, Sophie Veschambre, David Amouroux Bruno Bénech et Olivier F. X. Donard ; Platinum, Palladium, and Rhodium in Fresh Snow from the Aspe Valley (Pyrenees Mountains, France) ; Environ. Sci. Technol., 2007, 41 (1), pp 66–73 ; DOI :10.1021/es061483v, Résumé online 2006/12/02
- Carlo Barbante, Audrey Veysseyre, Christophe Ferrari, Katja Van De Velde, Christine Morel, Gabriele Capodaglio, Paolo Cescon, Giuseppe Scarponi et Claude Boutre ; http ://pubs. acs. org/doi/abs/10.1021/es000146y [Greenland Snow Evidence of Large Scale Atmospheric Contamination for Platinum, Palladium, and Rhodium] ; Environ. Sci. Technol., 2001, 35 (5), pp 835–839 ; DOI :10.1021/es000146y
- Sebastien Rauch, Harold F. Hemond, Carlo Barbante, Masanori Owari, Gregory M. Morrison, Bernhard Peucker-Ehrenbrink & Urban Wass ; Importance of Automobile Exhaust Catalyst Emissions for the Deposition of Platinum, Palladium, and Rhodium in the Northern Hemisphere ; Environmental Science & Technology2005 39 (21), 8156-8162
- R Djingova and P Kovacheva ; Analytical Problems and Validation of Methods for Determination of Palladium in Environmental Materials ; Palladium Emissions in the Environment ; 2006, 2, 145-162, DOI : 10.1007/3-540-29220-9_11
Liens externes
- (fr) Informations de marché sur le site de la Conférencedes nations unies sur le commerce et le développement : description, qualité, secteurs d'utilisation, marché, filière, sociétés, techniques, prix, politiques économiques
- (en) Los Alamos National Laboratory - Platinum
- (en) A balanced historical account of the sequence of discoveries of platinum; illustrated.
- (en) Animation présentant l'action de destruction de l'ADN d'une cellule (cancéreuse) par un oxyde de platine
- (en) WebElements. com - Platinum
- (en) EnvironmentalChemistry. com - Platinum
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC Press Inc, 2009, 90e éd. , Relié, 2804 p. (ISBN 978-1-420-09084-0)
- (en) Beatriz Cordero, Verónica Gómez, Ana E. Platero-Prats, Marc Revés, Jorge Echeverría, Eduard Cremades, Flavia Barragán et Santiago Alvarez, «Covalent radii revisited», dans Dalton Transactions, 2008, p. 2832 - 2838 [ lien DOI ]
- (en) Metals handbook, vol. 10 : Materials characterization, ASM International, 1986, 1310 p. (ISBN 0-87170-007-7) , p. 344
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, CRC, 2009, 89e éd. , p. 10-203
- «Platine» dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009
- Extrait de la thèse Équilibres oxydo-réducteurs dans les dichalcogénures de platine et de palladium. Influence de la pression sur la redistribution du nuage électronique de Céline Sortais-Soulard
- Note du BRGM pour le ministère de l'Industrie français
- Li, Ni, Pt, Pd : des métaux "critiques" ? ; notes de synthèse, rédigées par des experts d'IFP Energies nouvelles (PDF - 700 Ko)
- Avec le germanium (électronique avancée) ; le titane (sous-marins de chasse, alliage extrêmement résistant ; le magnésium (explosifs) ; le mercure (chimie nucléaire, instruments de mesure) ; le molybdène (acier) ; le cobalt (chimie nucléaire) ; le colombium (alliages spéciaux extrêmement rares). (Christine Ockrent, comte de Marenches, Dans le secret des princes, éd. Stock, 1986, p; 193. )
- Financial Times, 7 août 2008, page 14
- F. Alt, A. Bambauer, K. Hoppstock, B. Mergler and G. Tölg ; Platinum traces in airlimite particulate matter. Determination of whole content, particle size distribution and soluble platinum ; Fresenius'Journal of Analytical Chemistry ; Volume 346, Numbers 6-9, 693-696, DOI :10.1007/BF00321274 ; (Springerlink)
- Dagmar Laschka, Markus Nachtwey ; Platinum in municipal sewage treatment plants ; Chemosphere, Volume 34, Issue 8, April 1997, Pages 1803-1812
- Sonja Zimmermann & Bernd Sures ; 2004 ; Significance of platinum group metals emitted from automobile exhaust gas converters for the biosphere Sonja Zimmermann and Bernd Sures ; Environmental Science and Pollution Research Volume 11, Number 3, 194-199, DOI : 10.1007/BF02979675
- Jæ Sam Yang, Determination of palladium and platinum in seaweed ; Journal of Oceanography ; Volume 45, Number 6, Journal of Oceanography, 1989, Volume 45, Number 6, Pages 369-374 ; DOI : 10.1007/BF02125141
- R. Jouhaud, S. Biagianti-Risbourg, F. Arsac et G. Vernet ; Journal of Applied Ichthyology ; Volume 15, Issue 1, pages 41–48, Mars 1999; online : 2002/04/05 ; Résumé DOI : 10.1046/j. 1439-0426.1999.00114. x
- Rudi Schierl ;Environmental monitoring of platinum in air and urine ; Microchemical Journal, Volume 67, Issues 1-3, December 2000, Pages 245-248, doi :10.1016/S0026-265X (00) 00068-0 (Résumé)
- Sebastien Rauch, Bernhard Peucker-Ehrenbrink, Luisa T. Molina, Mario J. Molina, Rafæl Ramos, and Harold F ; Platinum Group Elements in Airlimite Particles in Mexico City. Hemond Environmental Science & Technology ; 2006 40 (24), 7554-7560
- Sebastien Rauch, Harold F. Hemond, Bernhard Peucker-Ehrenbrink, Kristine H. Ek, and Gregory M. Morrison ; Platinum Group Element Concentrations and Osmium Isotopic Composition in Urban Airlimite Particles from Boston, Massachusetts, Environmental Science & Technology ; 2005 39 (24), 9464-9470
- Cicchella D., De Vivo B. and Lima A ; [Palladium and platinum concentration in soils from the Napoli metropolitan area], Italy : envisageable effects of catalytic exhausts, The Science of the Total Environment, 308 : 121-131, online 21 February 2003.
- Andreas Limbeck, Christoph Puls, and Markus Handler ; [Platinum and Palladium Emissions from On-Road Vehicles in the Kaisermühlen Tunnel (Vienna, Austria) ] ; Environmental Science & Technology ; 2007 41 (14), 4938-4945
- Sebastien Rauch, Harold F. Hemond, & Bernhard Peucker-Ehrenbrink ; Recent Changes in Platinum Group Element Concentrations and Osmium Isotopic Composition in Sediments from an Urban Lake ; Environ. Sci. Technol., 2004, 38 (2), pp 396–402 ; DOI : 10.1021/es0347686
- Mariella Moldovan, Sophie Veschambre, David Amouroux Bruno Bénech et Olivier F. X. Donard ; Platinum, Palladium, and Rhodium in Fresh Snow from the Aspe Valley (Pyrenees Mountains, France) ; Environ. Sci. Technol., 2007, 41 (1), pp 66–73 ; DOI :10.1021/es061483v, Résumé online 2006/12/02
- Carlo Barbante, Audrey Veysseyre, Christophe Ferrari, Katja Van De Velde, Christine Morel, Gabriele Capodaglio, Paolo Cescon, Giuseppe Scarponi et Claude Boutre ; http ://pubs. acs. org/doi/abs/10.1021/es000146y [Greenland Snow Evidence of Large Scale Atmospheric Contamination for Platinum, Palladium, and Rhodium] ; Environ. Sci. Technol., 2001, 35 (5), pp 835–839 ; DOI :10.1021/es000146y
- Sebastien Rauch, Harold F. Hemond, Carlo Barbante, Masanori Owari, Gregory M. Morrison, Bernhard Peucker-Ehrenbrink & Urban Wass ; Importance of Automobile Exhaust Catalyst Emissions for the Deposition of Platinum, Palladium, and Rhodium in the Northern Hemisphere ; Environmental Science & Technology2005 39 (21), 8156-8162
- R Djingova and P Kovacheva ; Analytical Problems and Validation of Methods for Determination of Palladium in Environmental Materials ; Palladium Emissions in the Environment ; 2006, 2, 145-162, DOI : 10.1007/3-540-29220-9_11
| s1 | s2 | g | f1 | f2 | f3 | f4 | f5 | f6 | f7 | f8 | f9 | f10 | f11 | f12 | f13 | f14 | d1 | d2 | d3 | d4 | d5 | d6 | d7 | d8 | d9 | d10 | p1 | p2 | p3 | p4 | p5 | p6 | |
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Uut | Uuq | Uup | Uuh | Uus | Uuo | |
| 8 | Uue | Ubn | * | Ute | Uqn | Uqu | Uqb | Uqt | Uqq | Uqp | Uqh | Uqs | Uqo | Uqe | Upn | Upu | Upb | Upt | Upq | Upp | Uph | Ups | Upo | Upe | Uhn | Uhu | Uhb | Uht | Uhq | Uhp | Uhh | Uhs | Uho |
| ↓ | |||||||||||||||||||||||||||||||||
| g1 | g2 | g3 | g4 | g5 | g6 | g7 | g8 | g9 | g10 | g11 | g12 | g13 | g14 | g15 | g16 | g17 | g18 | ||||||||||||||||
| * | Ubu | Ubb | Ubt | Ubq | Ubp | Ubh | Ubs | Ubo | Ube | Utn | Utu | Utb | Utt | Utq | Utp | Uth | Uts | Uto | |||||||||||||||
| Métalloïdes | Non-métaux | Halogènes | Gaz rares |
| Métaux alcalins | Métaux alcalino-terreux | Métaux de transition | Métaux pauvres |
| Lanthanides | Actinides | Superactinides | Éléments non classés |
Recherche sur Google Images : |

"Platine Palladium, Palladium" L'image ci-contre est extraite du site platine-palladium.com Il est possible que cette image soit réduite par rapport à l'originale. Elle est peut-être protégée par des droits d'auteur. Voir l'image en taille réelle (389 × 488 - 95 ko - jpg)Refaire la recherche sur Google Images |
Recherche sur Amazone (livres) : |
Voir la liste des contributeurs.
La version présentée ici à été extraite depuis cette source le 09/12/2010.
Ce texte est disponible sous les termes de la licence de documentation libre GNU (GFDL).
La liste des définitions proposées en tête de page est une sélection parmi les résultats obtenus à l'aide de la commande "define:" de Google.
Cette page fait partie du projet Wikibis.




 Accueil
Accueil Recherche
Recherche Début page
Début page Contact
Contact Imprimer
Imprimer Accessibilité
Accessibilité